中学理科の定期テストでは、溶解度に関する問題が必ず出題されます。
特に、温度と溶解度の関係を表したグラフの読み取りや計算問題は、多くの生徒がつまずきやすいポイントです。
「何g溶けるのか分からない」
「水の量が変わると混乱する」
「グラフ問題になると手が止まる」
と感じている人も多いのではないでしょうか。
この記事では、定期テストで頻出の重要問題を中心に、
✔ 溶解度の意味と基本ルール
✔ 計算問題の考え方と解き方
✔ グラフ問題で失点しないコツ
を解説・解答付きでわかりやすくまとめています。
考え方が分かれば、溶解度は確実に得点できる単元です。テスト前の総復習にぜひ活用してください。
【問題】溶解度曲線の重要問題
下のグラフは、硝酸カリウムと塩化ナトリウムの溶解度曲線を表している。これについて、次の各問いに答えなさい。
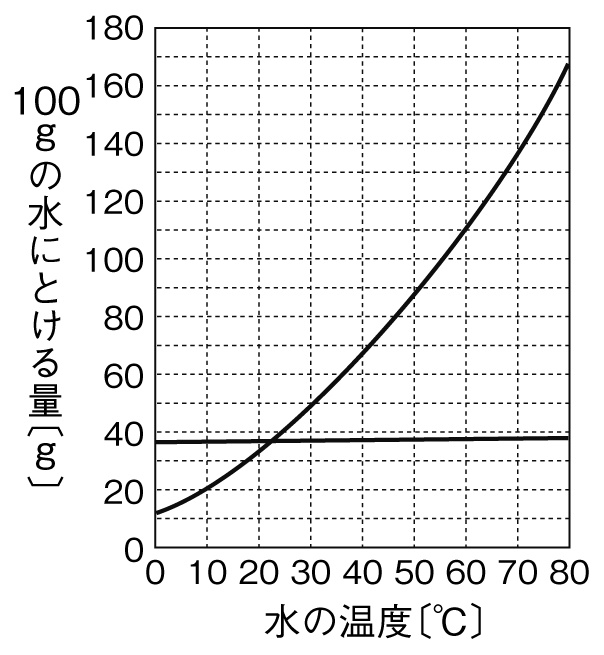
(1)60℃の水100gに硝酸カリウム80gを溶かして、硝酸カリウム水溶液をつくった。この水溶液を冷やしていくと、およそ何℃で結晶が出始めるか。
(2)(1)水溶液を10℃まで冷却すると、約何gの結晶が出てくるか。
(3)次に、60℃の水200gに硝酸カリウム130gを溶かして、硝酸カリウム水溶液をつくった。この水溶液の濃度は何%か。小数第一位を四捨五入し、整数で求めよ。
(4)(3)の水溶液が冷えて、硝酸カリウムが結晶になりはじめる温度は約何℃か。
(5)(3)の水溶液を0℃まで冷却すると、約何gの硝酸カリウムの結晶が出てくるか。
(6)60℃の水100gに塩化ナトリウムを溶けるだけ溶かし、60℃の飽和水溶液をつくった。その後、この飽和水溶液を20℃まで冷却したが、塩化ナトリウムの結晶ができるようすはほとんど観察できなかった。その理由を「溶解度」「温度」の2つのことばを用いて、簡潔に説明せよ。
【解答・解説】溶解度曲線の重要問題の解答
(1)約46℃
硝酸カリウム80gが溶解度になるのは、水の温度が約46℃になった時です。したがって、水の温度が46℃以下になると結晶ができ始めます。
(2)60g
10℃の硝酸カリウム水溶液の溶解度は約20gなので、溶けていた80gの硝酸カリウムのうち、
80g-20g=60g
約60gの結晶が出てきます。
(3)39%
まず、硝酸カリウム130gが、60℃の水200gにすべて溶けるかを確認します。60℃の水100gの硝酸カリウムの溶解度は、グラフより約110gであるとわかります。水の量はその2倍なので、約220gまで溶けることがわかります。したがって、硝酸カリウム130gはすべて溶けます。
質量パーセント濃度は、溶質/溶液 ×100 で求めることができるので、
130/(200+130) ×100=39.393…
小数第一位を四捨五入し、整数で求めると、約39%になります。
(4)約38℃
水100gのグラフ(溶解度のグラフ)なので、まず、水100gだったら何℃で結晶が出てくるか考えます。水200gに硝酸カリウム130gを溶かしたので、その半分の水100gに硝酸カリウム65gを溶かしたことと同じになります。これを冷却すると、約38℃で結晶が出てくるとわかります。
(5)約106g
水100gのグラフ(溶解度のグラフ)なので、まず、水100gだったら何gの結晶が出てくるか計算します。水200gに硝酸カリウム130gを溶かしたので、その半分の水100gに硝酸カリウム65gを溶かしたことと同じになります。これを0℃まで冷却すると、約12gしか硝酸カリウムが溶けないことがわかります。したがって、出てくる結晶の量は、
65g-12g=約53g
実際の水の量は、100gの2倍の200gなので、出てくる結晶の量も2倍になります。
53g×2=約106g
(6)塩化ナトリウムは水の温度が下がっても、溶解度があまり変化しないから。
塩化ナトリウム(食塩)は、水の温度が変化しても、溶解度があまり変化しない物質です。したがって、温度が下がっても結晶があまり出てきません。塩化ナトリウム水溶液から結晶をとり出すには、加熱し水を蒸発させる必要があります。

コメント